BAB I
PENDAHULUAN
A.
Latar
Belakang
Kromatografi
adalah teknik pemisahan fisik suatu campuran zat-zat kimia yang berdasar pada
perbedaan kecepatan migrasi dari masing-masing komponen campuran yang terpisah
pada fase diam dibawah pengaruh pergerakan fase yang bergerak. Kromatografi
bertujuan untuk pemisahan komponen dari matriks sampel dan tetap dibiarkan
dalam fase diam kemudian ditentukan untuk analisis.
Kromatografi
gas merupakan teknik instrumental yang dikenalkan pertama kali pada tahun
1950-an. Pekerjaan di laboratorium analisis pada umumnya tidak dapat dipisahkan
dengan proses pemisahan campuran zat-zat kimia, terutama apabila yang
dianalisis adalah suatu sampel dengan susunan yang kompleks. Cara-cara
pemisahan dan kecermatan pelaksanaan pemisahan campuran zat-zat. Di samping itu
metode analisis yang dipakai untuk penentuan zat kimia juga menuntut adanya
proses pemisahan sebelum dilakukan pengukuran kadar (secara kuantitatif) maupun
penentuan sifat fisika-kimia yang khas dari suatu zat yang akan ditentukan.
Maksud dan tujuan dilakukan pemisahan adalah untuk memisahkan komponen yang
akan ditentukan berada dalam keadaan murni tidak tercampur dengan
komponen-komponen yang lainnya.
Kromatografi gas (GC) merupakan salah satu teknik
spektroskopi yang menggunakan prinsip pemisahan campuran berdasarkan perbedaan
kecepatan migrasi komponen-komponen penyusunnya. Kromatografi gas ditemukan pada
tahun 1903 oleh Tswett dan biasa
digunakan untuk mengidentifikasi suatu senyawa yang terdapat pada campuran gas.
Pengidentifikasian secara lebih lanjut dapat digunakan dalam mengestimasi
konsentrasi suatu senyawa dalam fasa gas.
Kromatografi gas biasa digunakan untuk
mengidentifikasi suatu senyawa yang terdapat pada campuran gas dan juga mempunyai
peranan penting dalam mengestimasi konsentrasi suatu senyawa dalam fasa gas.
Data-data yang dihasilkan oleh detektor GC adalah kromatogram yang pembacaannya
memiliki fungsi tertentu tiap spesifikasinya.
Kromatografi
gas merupakan salah satu jenis teknik analisis yang semakin banyak diamati,
karena terbukti dapat digunakan untuk menyelesaikan berbagai masalah analisis.
Pada awalnya (GC) hanya digunakan untuk analisis gas saja. Akan tetapi dengan
kemajuan ilmu dan teknologi, akhirnya (GC) dapat digunakan untuk analisis bahan
cair dan padat termasuk bahan polimer.
Sekarang ini, kromatografi sangat diperlukan dalam kefarmasian dalam
memisahkan suatu campuran senyawa. Dalam kromatografi, komponen-komponen
terdistribusi dalam dua fase. Salah satu fase adalah fase diam. Transfer massa
antara fase bergerak dan fase diam terjadi bila molekul-molekul campuran serap
pada permukaan partikel-partikel atau terserap di dalam pori-pori partikel atau
terbagi kedalam sejumlah cairan yang terikat pada permukaan atau di dalam pori.
Kromatografi gas merupakan teknik analisis yang telah digunakan dalam bidang:
industri, farmasi, kimia, klinik, forensik, makanan, dll. (Himawan, 2009).
Kromatografi
gas juga merupakan metode yang tepat dan cepat untuk memisahkan campuran yang
sangat rumit. Waktu yang dibutuhkan beragam, mulai dari beberapa detik utnuk
campuran sederhana sampai berjam-jam untuk campuran yang mengandung 500-1000
komponen. Komponen campuran dapat diidentifikasikan dengan menggunakan waktu
tambat (waktu retensi) yang khas pada kondisi yang tepat. Waktu tambat ialah
waktu yang menunjukkan berapa lama suatu senyawa tertahan dalam kolom.waktu
tambat diukur dari jejak pencatat pada kromatogram dan serupa dengan volume
tambat dalam KCKT dan Rf dalam KLT. Dengan kalibrasi yang patut, banyaknya
(kuantitas) komponen campuran dapat pula diukur secara teliti . kekurangan
utama KG adalah bahwa ia tidak mudah dipakai untuk memisahkan campuran dalam
jumlah besar. Pemisahan pada tingkat mg mudah dilakukan, pemisahan campuran pada
tingkat g mungkin dilakukan; tetapi pemisahan dalam tingkat pon atau ton sukar
dilakukan kecuali jika tidak ada metode lain. (Puspita, 2007).
B.
Tujuan
Adapun
tujuan pada percobaan ini yaitu sebagai berikut:
1. Mempelajari
instrumen pada metode kromatografi gas.
2. Memisahkan
komponen menggunakan kromatografi gas.
BAB II
PEMBAHASAN
A.
Pengertian dan Prinsip Kromatografi Gas
Kromatografi gas adalah suatu metode
analisis yang didasarkan pemisahan fisik zat organic atau anorganik yang stabil
pada pemanasan dan mudah diatsirikan. Pada umumnya kegunaan kromatografi gas
adalah untuk melakukan pemisahan dan identifikasi senyawa yang mudah menguap
dan juga untuk melakukan analisis kualitatif dan kuantitatif senyawa dalam campuran. Dalam kromatografi gas, fase
bergeraknya adalah gas dan zat terlarut terpisah sebagai uap. Pemisahan
tercapai dengan partisi sampel antara fase gas bergerak dan fase diam berupa
cairan dengan titik didih tinggi (tidak mudah menguap) yang terikat pada zat
padat penunjangnya.
GC menggunakan gas
sebagai gas pembawa/fase geraknya. Ada 2 jenis kromatografi gas, yaitu :
1. Kromatografi gas–cair (KGC) yang fase diamnya berupa
cairan yang diikatkan pada suatu pendukung sehingga solut akan terlarut dalam
fase diam.
2. Kromatografi gas-padat (KGP), yang fase diamnya
berupa padatan dan kadang-kadang berupa polimerik.
Prinsip kromatografi gas: Pada dasarnya
prinsip yang digunakan pada kromatografi gas dan HPLC secara garis besar adalah
sama karena sama-sama menggunakan kolom, hanya saja pada kromatografi gas,
sampel yang diinjeksikan harus yang tahan panas karena menggunakan gas
pembakar. Disamping itu pada kromatografi gas, selain oleh afinitasnya terhadap
fase diam maupun fase gerak, pemisahannya juga ditentukan oleh titik didih
keatsirian dari sampel.
Fase Diam Dan Fase
Gerak Pada Kromatografi Gas
1)
Fase
Diam
Pemilihan fasa diam juga harus
disesuaikan dengan sampel yang akan dipisahkan. Untuk sampel yang bersifat
polar sebaiknya digunakan fasa diam yang polar. Begitupun untuk sampel yang
nonpolar, digunakan fasa diam yang nonpolar agar pemisahan dapat berlangsung
lebih sempurna.
Fase
diam pada Kromatografi Gas biasanya berupa cairan yang disaputkan pada bahan
penyangga padat yang lembab, bukan senyawa padat yang berfungsi sebagai
permukaan yang menyerap (kromatografi gas-padat). Sistem gas-padat telah
dipakai secara luas dalam pemurnian gas dan penghilangan asap, tetapi kurang
kegunaannya dalam kromatografi. Pemakaian fase cair memungkinkan kita memilih
dari sejumlah fase diam yang sangat beragam yang akan memisahkan hampir segala
macam campuran.
2)
Fase
Gerak
Disebut
juga sebagai gas pembawa. Fungsi utamanya adalah untuk membawa uap analit
melalui system kromatografi tanpa berinteraksi dengan komponen-komponen sampel.
Adapun
syarat-syarat fase gerak pada kromatografi gas yaitu sebagai berikut::
- Tidak reaktif
- Murni (agar tidak mempengaruhi detector)
- Dapat disimpan dalam tangki tekanan
tinggi. Biasanya mengandung gas helium, nitrogen, hydrogen, atau campuran argon
dan metana
-
Pemilihan gas pembawa yang digunakan
tergantung dari detektor apa yang digunakan
B.
Komponen
dalam Kromatografi Gas
Adapun komponen-komponen dari
kromatografi gas yaitu sebagai berikut :
1.
Gas
Pembawa
Pada
pengamatan ini, terlihat tiga tabung gas yang memiliki warna yang berbeda. Pada
tabung 1, berisi gas tekan; tabung 2, berisi gas Nitrogen (N2) dan
pada tabung 3, berisi gas Hidrogen (H2).
Gas
pembawa harus bersifat inert artinya gas ini tidak bereaksi dengan cuplikan
ataupun fasa diamnya. Gas ini disimpan dalam silinder baja bertekanan tinggi
sehingga gas ini akan mengalir cepat dengan sendirinya. Karena aliran gas yang
cepat inilah maka pemisahan dengan kromatografi gas berlangsung hanya dalam
beberapa menit saja.
Gas
pembawa yang biasa digunakan adalah gas argon, helium, hidrogen dan nitrogen.
Gas nitrogen memerlukan kecepatan alir yang lambat (10 cm/detik) untuk mencapai
efisiensi yang optimum dengan HETP (High Eficiency Theoretical Plate) minimum.
Sementara hidrogen dan helium dapat dialirkan lebih cepat untuk mencapai
efisiensi optimumnya, 35 cm/detik untuk gas hidrogen dan 25 cm/detik untuk
helium. Dengan kenaikan laju alir, kinerja hidrogen berkurang sedikir demi
sedikit sedangkan kinerja nitrogen berkurang secara drastis.
Semakin
cepat solut berkesetimbangan di antara fasa diam dan fasa gerak maka semakin
kecil pula faktor transfer massa. Difusi solut yang cepat membantu mempercepat
kesetimbangan di antara dua fasa tersebut, sehingga efisiensinya meningkat
(HETP nya menurun). Pada kecepatan alir tinggi, solut berdifusi lebih cepat
melalui hidrogen dan helium daripada melalui nitrogen. Hal inilah yang
menyebabkan hidrogen dan helium memberikan resolusi yang lebih baik daripada
nitrogen. Hidrogen memiliki efisiensi yang relatif stabil dengan adanya
perubahan kecepatan alir. Namun, hidrogen mudah meledak jika terjadi kontrak
dengan udara. Biasanya, helium banyak digunakan sebagai penggantinya. Kotoran yang terdapat dalam carrier gas dapat bereaksi
dengan fasa diam. Oleh karena itu, gas yang digunakan sebagai gas pembawa yang
relatif kecil sehingga tidak akan merusak kolom. Biasanya terdapat saringan
(molecular saeive) untuk menghilangkan kotoran yang berupa air dan hidrokarbon
dalam gas pembawa . Pemilihan gas pembawa biasanya disesuaikan dengan jenis
detektor.
2.
Injektor
Sampel
dapat berupa gas atau cairan dengan syarat sampel harus mudah menguap saat
diinjeksikan dan stabil pada suhu operasional (50°-300° C). Injektor berada
dalam oven yang temperaturnya dapat dikontrol. Suhu injektor biasanya 50° C di
atas titik didih cuplikan. Jumlah cuplikan yang diinjeksikan sekitar 5 µL.
Tempat pemasukkan cuplikan cair pada kolom pak biasanya terbuat dari tabung
gelas di dalam blok logam panas. Injeksi sampel menggunakan semprit kecil.
Jarum semprit menembus lempengan karet tebal disebut septum yang mana akan
mengubah bentuknya kembali secara otomatis ketika semprit ditarik keluar.
Untuk
cuplikan berupa gas dapat dimasukkan dengan menggunakan alat suntik gas
(gas-tight syringe) atau kran gas (gas-sampling valve). Alat pemasukan cuplikan
untuk kolom terbuka dikelompokkan ke dalam dua kategori yaitu injeksi split
(split injection) dan injeksi splitless (splitless injection). Injeksi split
dimaksudkan untuk mengurangi volume cuplikan yang masuk ke kolom. Cuplikan yang
masuk biasanya hanya 0,1 % hingga 10 %
dari 0,1-2 µL, sementara sisanya dibuang.
Gambar 1.2 Sistem injeksi split
Sedangkan injeksi splitless lebih
cocok digunakan untuk analisa renik.
3.
Kolom
Kolom
pada umumnya terbuat dari baja tahan karat atau terkadang dapat terbuat dari
gelas. Kolom kaca digunakan bila untuk memisahkan cuplikan yang mengandung
komponen yang dapat terurai jika kontak dengan logam. Diameter kolom yang
digunakan biasanya 3 mm – 6 mm dengan panjang antara 2-3 m. kolom dibentuk
melingkar agar dapat dengan mudah dimasukkan ke dalam oven ( thermostat ).
Kolom
adalah tempat berlangsungnya proses pemisahan komponen yang terkandung dalam
cuplikan. Di dalam kolom terdapat fasa diam yang dapat berupa cairan, wax, atau
padatan dengan titik didih rendah. Fasa diam ini harus sukar menguap, memiliki
tekanan uap rendah, titik didihnya tinggi (minimal 100º C di atas suhu operasi
kolom) dan stabil secara kimia. Fasa diam ini melekat pada adsorben. Adsorben
yang digunakan harus memiliki ukuran yang seragam dan cukup kuat agar tidak
hancur saat dimasukkan ke dalam kolom. Adsorben biasanya terbuat dari celite
yang berasal dari bahan diatomae. Cairan yang digunakan sebagai fasa diam di antaranya adalah
hidrokarbon bertitik didih tinggi, silicone oils, waxes, ester polimer, eter
dan amida. (The Techniques). Pemilihan fasa diam juga harus disesuaikan dengan
sampel yang akan dipisahkan. Untuk sampel yang bersifat polar sebaiknya
digunakan fasa diam yang polar. Begitupun untuk sampel yang nonpolar, digunakan
fasa diam yang nonpolar agar pemisahan dapat berlangsung lebih sempurna.
Ada
dua tipe kolom yang biasa digunakan dalam kromatografi gas, yaitu kolom pak
(packed column) dan kolom terbuka (open tubular column).
-
Kolom
pak (packed column)
Kolom
pak terbuat dari stainless steel atau gelas Pyrex. Gelas Pyrex digunakan jika
cuplikan yang akan dipisahkan bersifat labil secara termal. Diameter kolom pak
berkisar antara 3 – 6 mm dengan panjang 1 – 5 m. kolom diisi dengan zat padat
halus sebagai zat pendukung dan fasa diam berupa zat cair kental yang melekat
pada zat pendukung. Kolom pak dapat menampung jumlah cuplikan yang banyak
sehingga disukai untuk tujuan preparatif. Kolom yang terbuat dari stainless
steel biasa dicuci dengan HCl terlarut, kemudian ditambah dengan air diikuti
dengan methanol, aseton, metilen diklorida dan n-heksana. Proses pencucian ini
untuk menghilangkan karat dan noda yang berasal dari agen pelumas yang
digunakan saat membuat kolom. Kolom pak diisi dengan 5% polyethylene glycol
adipate dengan efisiensi kolom sebesar 40,000 theoretical plates
-
Kolom terbuka (open tubular column)
Kolom terbuka terbuat dari stainless
steel atau quartz. Berdiameter antara 0,1 – 0,7 mm dengan panjang berkisar
antara 15 - 100 m. semakin panjang kolom maka akan efisiensinya semakin besar
dan perbedaan waktu retensi antara komponen satu dengan komponen lain semakin
besar dan akan meningkatkan selektivitas. Penggunaan kolom terbuka memberikan
resolusi yang lebih tinggi daripada kolom pak. Tidak seperti pada kolom pak,
pada kolom terbuka fasa geraknya tidak mengalami hambatan ketika melewati kolom
sehingga waktu analisis menggunakan kolom ini lebih singkat daripada jika
menggunakan kolom pak.
4. Termostat (Oven)
Termostat
(oven) adalah tempat penyimpanan kolom. Suhu kolom harus dikontrol. Temperatur
kolom bervariasi antara 50ºC - 250ºC. Suhu injektor lebih rendah dari suhu
kolom dan suhu kolom lebih rendah daripada suhu detektor. Suhu kolom optimum
bergantung pada titik didih cuplikan dan derajat pemisahan yang diinginkan.
Operasi
GC dapat dilakukan secara isotermal dan terprogram. Analisis yang dilakukan
secara isotermal digunakan untuk memisahkan cuplikan yang komponen-komponen
penyusunnya memiliki perbedaan titik didih yang dekat, sedangkan sistem
terprogram digunakan untuk memisahkan cuplikan yang perbedaan titik didihnya
jauh.
5. Detektor
Detektor adalah komponen yang
ditempatkan pada ujung kolom GC yang menganalisis aliran gas yang keluar dan
memberikan data kepada perekam data yang menyajikan hasil kromatogram secara
grafik. Detektor menunjukkan dan mengukur jumlah komponen yang dipisahkan oleh
gas pembawa. Alat ini akan mengubah analit yang telah terpisahkan dan dibawa
oleh gas pembawa menjadi sinyal listrik yang proporsional. Oleh karena itu,
alat ini tidak boleh memberikan respon terhadap gas pembawa yang mengalir pada
waktu yang bersamaan. Beberapa detektor yang dapat digunakan antara lain:
detektor hantar bahang (DHB), detektor ionisasi nyala (FID), detektor tangkap
ion, dan lain sebagainya.
6. Rekorder
Rekorder
berfungsi sebagai pencetak hasil percobaan pada lembaran kertas berupa kumpulan
puncak, yang selanjutnya disebut sebagai kromatogram. Seperti telah
diberitahukan diawal, jumlah puncak dalam kromatogram menyatakan jumlah
komponen penyusun campuran. Sedangkan luas puncak menyatakan kuantitas
komponennya.
C.
Cara Menjalankan alat GC
Berdasarkan pengamatan yang
dilakukan, dapat diketahui tahap-tahap dalam menjalankan alat GC tersebut.
Yaitu:
1. Mengaktifkan
dan melakukan pemanasan terhadap alat sebelum dipergunakan dengan cara menekan
tombol power dan mendiamkan selama ± 15 menit.
2. Mengalirkan
gas menuju injektor dengan cara memutar knop yang terdapat pada tabung gas.
3. Melakukan
pengaturan suhu pada detektor dengan cara menekan tombol DET lalu mengatur suhu
sebesar 100oC kemudian menekan tombol OK.
4. Melakukan
pengaturan suhu pada injektor dengan cara menekan tombol INJ lalu mengatur suhu
sebesar 150oC kemudian menekan tombol OK.
5. Melakukan
pengaturan suhu pada kolom dengan cara menekan tombol COL lalu mengatur suhu
sebesar 200oC kemudian menekan tombol OK.
6. Mengaktifkan
Detektor apabila telah tercapai suhu yang dikehendaki. Hal ini dapat dilakukan
dengan cara memasukkan api ke dalam lubang detektor.
7. Melakukan
pengujian terhadap detektor untuk mengetahui proses pembakaran telah
berlangsung. Hal ini dilakukan dengan cara menempelkan sebuah pada lubang
bagian atas dan mengamati apakah terdapat butiran embun atau tidak. Apabila
terdapat butiran embun maka alat detektor sudah siap digunakan.
8. Mengambil
sampel dan memasukkannya ke dalam injektor dengan bantuan alat syringe.
9. Menekan
tombol spasi pada alat komputerisasi bersamaan dengan memasukkan sampel,
kemudian melihat hasil kromatografi.
10. Mengamati
kromatogram dan menetukan waktu retensi (tR) sampel.
D.
Mekanisme
Kerja Dalam Kromatografi Gas
Pada percobaan ini, akan dilakukan pemisahan komponen-komponen
pada larutan n-Heksana. N-Heksana dapat dideteksi dikarenakan senyawa ini
merupakan senyawa organik yang memiliki titik didih cukup rendah dan bersifat
volatil.
Adapun mekanisme kerja kromatografi gas
adalah sebagai berikut : gas bertekanan tinggi dialirkan ke dalam kolom yang
berisi fasa diam, kemudian sampel berupa n-Heksana diinjeksikan ke dalam aliran
gas dan ikut terbawa oleh gas ke dalam kolom. Di dalam kolom
akan terjadi proses pemisahan dari n-Heksana menjadi komponen-komponen
penyusunnya. Komponen-komponen tersebut satu per satu
akan keluar kolom dan mencapai detektor yang diletakkan di ujung akhir kolom. Hasil pendeteksian direkam oleh rekorder dan dikenal sebagai kromatogram. Jumlah peak
pada kromatogram menyatakan jumlah komponen yang terdapat
dalam cuplikan dan kuantitas suatu komponen ditentukan berdasarkan
luas peaknya.
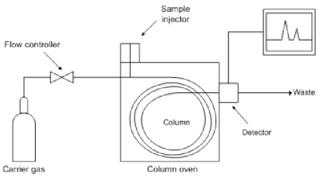
Berikut adalah skema
dari instrumen GC:
Gambar Diagram kromatografi gas
Adapun hasil yang diperoleh
pada pemisahan komponen n-Heksana ini, dapat dilihat dalam bentuk kromatogram
sebagai berikut:
Pada
gambar di atas, dapat dilihat sebuah kromatogram sederhana yang memiliki 3
puncak. Puncak kecil yang berada di kiri merepresentasikan spesies yang tidak
ditahan oleh fasa diam. Waktu (tM) setelah injeksi sampel sampai
dengan munulnya puncak ini seringkali dinamakan waktu mati (dead time). Waktu
mati memberikan pengukuran dari laju migrasi rata-rata dari fasa bergerak dan
merupakan suatu parameter yang penting dalam mengidentifiasi puncak analit.
Seringkali suatu sampel akan mengandung spesies yang tidak ditahan, jika mereka
tidak memiliki spesies yang tidak ditahan maka penambahan spesies dengan sifat
seperti ini dapat dilakukan untuk membantu identifikasi puncak.
Puncak
lebih besar yang terdapat di bagian tengah gambar di atas, merupakan puncak
dari spesies analit yaitu berupa n-Heksana. Waktu yang diperlukan puncak ini
untuk mencapai detektor atau waktu yang diperlukan spesies analit untuk keluar
dari kolom dan mencapai detektor dinamakan waktu retensi (tR). Adapun
nilai Rf dari n-Heksana yaitu 1,433. Berikut nilai waktu retensi dari
komponen-komponen n-Heksana yang terbaca oleh alat GC ini:
F.
Kelebihan
dan Kekurangan Kromatografi Gas
Adapun kelebihan dan kekurangan dalam penggunaan
metode pemisahan berdasarkan kromatografi gas (GC) yaitu sebagai berikut:
- Kelebihan:
1. Waktu analisis yang singkat dan
ketajaman pemisahan yang tinggi.
2. Dapat menggunakan kolom lebih
panjang untuk menghasilkan efisiensi pemisahan yang tinggi.
3. Gas mempunyai vikositas yang rendah.
4. Kesetimbangan partisi antara gas dan
cairan berlangsung cepat sehingga analisis relatif cepat dan sensitifitasnya
tinggi.
5. Pemakaian fase cair memungkinkan
kita memilih dari sejumlah fase diam yang sangat beragam yang akan memisahkan
hampir segala macam campuran.
- Kekurangan:
1. Teknik kromatografi gas terbatas
untuk zat yang mudah menguap.
2. Kromatografi gas tidak mudah dipakai
untuk memisahkan campuran dalam jumlah besar. Pemisahan pada tingkat mg mudah
dilakukan, pemisahan pada tingkat gram mungkin dilakukan, tetapi pemisahan
dalam tingkat pon atau ton sukar dilakukan kecuali jika ada metode lain.
3. Fase gas dibandingkan sebagian besar
fase cair tidak bersifat reaktif terhadap fase diam dan zat terlarut.
BAB III
KESIMPULAN
Berdasarkan tujuan dan hasil pengamatan
dapat ditarik kesimpulan sebagai berikut:
1. Prinsip
dasar metode kromatografi gas adalah pemisahan komponen-komponen dalam suatu
campuran berdasarkan kepolarannya. Dimana komponen yang memiliki kedekatan
polaritas dengan fasa diam maka akan tertahan di kolom, sedangkan komponen yang
memiliki kedekatan polaritas dengan fasa gerak
akan terelusi keluar dari kolom (keluar duluan).
2. Komponen-komponen
utama instrumen GC yaitu: Gas Pembawa, Detektor, Kolom, Injektor, Rekorder dan
Komputer (Penampil Kromatogram).
3. Adapun
kelebihan dan kekurangan dari penggunaan metode pemisahan menggunakan
kromatografi gas yaitu sebagai berikut:
- Kelebihan:
1. Waktu analisis yang singkat dan
ketajaman pemisahan yang tinggi.
2. Dapat menggunakan kolom lebih
panjang untuk menghasilkan efisiensi pemisahan yang tinggi.
3. Gas mempunyai vikositas yang rendah.
4. Kesetimbangan partisi antara gas dan
cairan berlangsung cepat sehingga analisis relatif cepat dan sensitifitasnya
tinggi.
5. Pemakaian fase cair memungkinkan
kita memilih dari sejumlah fase diam yang sangat beragam yang akan memisahkan
hampir segala macam campuran.
- Kekurangan:
1. Teknik kromatografi gas terbatas
untuk zat yang mudah menguap.
2. Kromatografi gas tidak mudah dipakai
untuk memisahkan campuran dalam jumlah besar.
3. Fase gas dibandingkan sebagian besar
fase cair tidak bersifat reaktif terhadap fase diam dan zat terlarut.
DAFTAR
PUSTAKA
Anonim.
2009. Kromatografi Gas-Cair.
http://www.chem-is-try.org/kromatografi_gas_cair.html. Diunduh 17
Juni 2012.
Anwar, Chairil. 1994. Pengantar Praktikum Kimia
Organik. UGM-Press. Yogyakarta.
Himawan,
Joseph. 2007. Kromatografi Gas.
http://tupai-terbang.blogspot.com/kromatografi_gas.html. Diunduh 17 Juni 2012.
Puspita, Dewi.
2007. Kromatografi Gas. http://the_doctor.blogspot.com/kromatografi_gas.html. Diunduh 17 Juni 2012.








Tidak ada komentar:
Posting Komentar